Биология для 9 класса — Асанов Н.

| Название: | Биология для 9 класса |
| Автор: | Асанов Н., Соловьева А., Ибраимова Б. |
| Жанр: | Школьный учебник по биологии |
| Издательство: | Атамура |
| Год: | 2019 |
| ISBN: | 978-601-331-594-2 |
| Язык книги: | Русский |
Страница - 7
Глава 4. ПИТАНИЕ
§ 10. Процесс пищеварения и роль ферментов в нем
Цель изучения этой темы описать в деталях процессы пищеварения у человека; установить взаимосвязь между органическим веществом и соответствующим ферментом в процессе переваривания пищи.
Как организм человека получает и использует органические вещества? Как связаны дыхание и пищеварение? Сколько энергии получает наш организм при распаде 1 г белков, жиров и углеводов? Из каких компонентов состоят белки, жиры и углеводы? Назовите органы пищеварительного тракта человека Какие структуры находятся в ротовой полости, для чего они нужны? В коком отделе пищеварительной системы происходит основной процесс всасывания в кровь переваренных органических веществ? Какие вещества не перевариваются в органах пищеварения, в каком отделе они попадают в кровь?
Что нужно повторить для успешного изучения темы? § 14 и 24 - учебник для 7 класса: § 3-5, 11-12 - учебник для 8 класса.
Пищеварение у человека, как и у большинства высокоорганизованных животных, включает в себя три процесса: физический (измельчение нищи), химический (нереваривание пищи под действием пищеварительных соков) и физиологический (всасывание питательных веществ в кровь). Два последних процесса называют секрецией и абсорбцией. Пищеварение - это усвоение организмом питательных веществ, процесс, в результате которого белки, жиры и углеводы пищи превращаются в вещества, способные попасть в кровь и разноситься по клеткам нашего организма. То есть его можно разделить на переваривание питательных веществ и их адсорбцию - всасывание в кровь. Переваривание включает в себя механическую (пережевывание) и химическую (разложение под действием специальных пищеварительных ферментов) обработку пищи. Что же такое ферменты? Это особые белки-катализаторы, которые могут в сотни и тысячи раз ускорять химические реакции. Причем многие реакции без ферментов вообще не будут происходить. Пищеварительные ферменты - это белки, ускоряющие реакции разложения пищи, т. е. переваривание органических веществ. Вспомните роль лизосом в клетке. Лизосомы заполнены ферментами, способными разлагать, разрушать, переваривать различные вещества.
Всасывание, или адсорбция, - это физиологический процесс прохождения мелких молекул органических веществ, образовавшихся в ходе переваривания, через клетки кишечника в кровь и лимфу (рис. 17).
Органы пищеварения делятся на две большие группы: пищеварительный тракт и пищеварительные железы. Как вы помните, первый
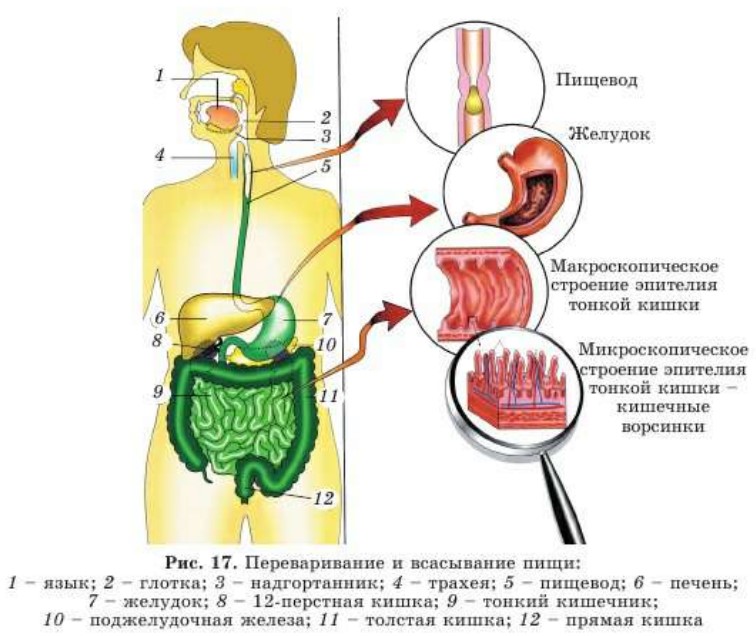
отдел пищеварительного тракта - ротовая полость. Во рту: 1) пища измельчается с помощью зубов (пережевывается), 2) пища смачивается слюной, 3) уничтожаются некоторые бактерии, 4) определяется вкус и температура пищи. Но самое главное - здесь разлагаются углеводы! Это происходит под действием основного фермента слюны амилазы, которая разлагает крахмал до глюкозы. Фермент мальтаза катализирует разложение солодового сахара - мальтозы. А под действием вещества лизоцима уничтожаются некоторые вредные бактерии.
Глотка и пищевод - полые органы с хорошо развитым мышечным слоем, проводят пищу из ротовой полости в желудок.
Глотка - общий отдел дыхательной и пищеварительной системы. На входе в гортань находится хрящ - надгортанник, который не позволяет пище туда попасть (подавиться). В верхней трети пищевода (как и в глотке) расположены поперечно полосатые мышцы. Их сокращения особенно важны при продвижении крупных твердых кусков пищи. Внутренний эпителиальный слой пищевода выделяет слизь, не содержащую ферментов, но облегчающую скольжение - продвижение пищи.
Желудок - расширение пищевого канала. Его особенность - растяжимость. Достигается она за счет складок в слизистой оболочке. Стенки желудка содержат три слоя гладких мышц, что обеспечивает сокращение во всех направлениях и перемешивание пищи с желудочным соком. В эпителии находится множество одноклеточных желез, выделяющих желудочный сок (до 2 л в сутки). В его состав входят слизь (защита от са- мопереваривания), фермент пепсин (разложение белков до аминокислот), соляная киcлота (для активации пепсина).
Из желудка пища понадает в первый отдел тонкого кишечника - двенадцатиперстную кишку. В нее открываются протоки печени и поджелудочной железы. Печень выделяет желчь. Как она участвует в превращении, мы рассмотрим в следующих параграфах. Поджелудочная железа (лат. pancreas) выделяет в кишечник пищеварительный панкреатический сок, который содержит несколько ферментов. Главный фермент панкреатического сока - липаза. Она расщепляет жиры до глицерина и жирных кислот. Кроме нее есть фермент трипсин, допереваривающий белки, и амилаза, допереваривающая углеводы. Следует помнить, что без желчи липаза "не работает".
Остальные отделы тонкого кишечника всасывают переваренные вещества в кровь и лимфу через микроскопические выросты - кишечные ворсинки. Результаты расщепления белков и углеводов - аминокислоты и глюкоза - всасываются в кровь. А вот глицерин и жирные кислоты, образовавшиеся при переваривании жиров, попадают в лимфу, преобразуются и ею транспортируются.
В толстом кишечнике в кровь всасываются вода, витамины и минеральные соли, которые не переварились. Кроме того, здесь разлагается растительная клетчатка под влиянием симбиотических бактерий - кишечной палочки. Непереваренные остатки пищи выводятся из организма через последний отдел толстого кишечника - прямую кишку.
На границе между толстой и тонкой кишкой находится слепой выроет - апендикс.
Действие основных пищеварительных ферментов можно изобразить в виде схемы:

Знание и понимание
- Объясните, когда, где и как происходит всасывание питательных веществ в кровь и лимфу.
- Объясните, где и как перевариваются белки, жиры и углеводы.
Применение
- Опишите функции липазы, пепсина и амилазы, трипсина, лизоцима.
- Определите связь между отделом пищеварительного канала и его функциями; пищеварительной железой и ее ферментами.
Анализ
- Проанализируйте все этапы и процессы, происходящие с пищей: химические, физические и физиологические.
- Покажите разницу между секрецией и адсорбцией. Проанализируйте и установите зависимость между ними, органами пищеварения и типом воздействия на пищу: механическим (физическим), химическим (ферментативным) и физиологическим.
Синтез
- Составьте схему «Преобразование веществ в органах пищеварения».
- Установите взаимосвязь между от- делом пищеварительного канала, его кислотностью, железой, ферментом и преобразованием питательных веществ.

Оценка
- Оцените представ ленный график зависимости активности ферментов от кислотности среды. Можно ли определить, где какой фермент, если предположить, что на графике изображены пепсин, трипсин и амилаза? Какие выводы можно сделать на основании данного графика?
- Оцените значение мутации, в результате которой у человека появился бы пищеварительный фермент, способный с легкостью превращать целлюлозу в глюкозу.
§ 11. Механизм действия ферментов
Цель изучения этой темы: изучить механизм действия ферментов.
Какие реакции в химии называются каталитическими? Как и почему организм травоядных может усваивать растительную пищу? Почему организм хищников к этому не способен? Откуда берутся белки в наших клетках и организме, в том числе и белки-ферменты?
Что нужно повторить для успешного изучения темы? Материал по химии о катализаторах.
Механизмы работы катализаторов. Вспомним из курса химии: катализаторы - это вещества, ускоряющие химических реакции, но не расходующиеся в ходе этих реакций. В популярной литературе можно встретить такое определение: катализаторы - это вещества, ускоряющие химические реакции, но сами в них не участвующие. Это определение верно, только если рассматривать конечные результаты химической реакции. То есть в конце реакции количество катализатора будет таким же, как и до вступления в реакцию. Произойдет химическое изменение других веществ (их соединение или разложение), но количество катализатора не изменится. Что такое химическая реакция? Это взаимодействие веществ, в результате которого появляются новые вещества. Если обозна чить какие-либо вещества латинскими буквами, то реакция соединения будет выглядеть так: А+В—>АВ, реакция замещения: АВ+СЕ—»АС+ВЕ, а реакции разложения: АВ—>А+В.
Вещества, вступающие в химическую реакцию, называются реагентами, а вещества, образующиеся в результате, - ее продуктами. В химии, да и в физике, важнейшими показателями являются скорость и равновесие химической реакции. Равновесие - это химическое понятие, характерное для обратимых химических реакций. Оно показывает соотношение между количеством реагентов и продуктов реакции, образующимися в каждую единицу времени: А+В⇄АВ. Часто катализаторы увеличивают именно скорость одной из реакций, сдвигая ее равновесие в ту или иную сторону.
Катализ - это увеличение скорости химической реакции в присутствии катализатора. Часто катализаторы способны повышать скорость преобразования химических веществ в десятки, сотни и, вероятно, в тысячи раз! Как же это происходит? Сначала катализатор вступает в реакцию с одним из веществ, после чего эта временная химическая структура взаимодействует с другим веществом. Молекулы реагентов, начавшие взаимодействовать друг с другом, как бы "отпускают" молекулы катализатора, который вытесняется из реакции и в конце остается неизменным. Если обозначить катализатор буквой К. то его роль можно отразить в виде следующей схемы: А + К = АК; АК + В = АВ + К.
Причем, если эта реакция каталитическая, взаимодействие веществ А и В либо вообще не происходит (!), либо происходит так медленно, что результаты этой реакции не обнаруживаются обычными способами.
Механизм действия ферментов. Как вы помните, ферменты — это биологические катализаторы. Как работают ферменты? Их участие в химических реакциях ничем принципиально не отличается от роли любых других катализаторов. То есть ферменты действуют так же, как и другие

Что еще есть общего в механизмах действия обычных неорганических катализаторов и ферментов?
- Огромное количество реакций может быть ускорено с помощью ферментов. Так, по мнению ученых-химиков, изучающих катализ, «научнотехнический опыт показывает, что для любой реакции можно подобрать катализатор».
- Скорость каталитических реакций зависит также от других условий: температуры, давления, концентрации вещества, площади их соприкосновения и т. д.
- Ферменты, как и катализаторы, участвующие в обратимых реакциях, не просто повышают их скорость, а существенно сдвигают равновесие в сторону повышения количества результатов продуктов реакции, а не их исходных реагентов.
Теперь рассмотрим некоторые важные особенности органических катализаторов.
- Высокая специфичность. Часто (но не всегда) фермент способен контролировать, т. е. ускорять только одну какую-либо химическую реакцию. Неорганические вещества (серная кислота, цинк, платина и др.) ускоряют многие химические реакции, работая как катализаторы.
- По своей химической природе большинство ферментов белки, т. е. сложные органические вещества. Зачастую ферменты включают в себя очень большое количество мономеров либо состоят из отдельных субъединиц, собирающихся вместе для осуществления катализа. Хотя в живом организме иногда работает небольшое количество относительно простых «небелковых» катализаторов.
- Ферменты работают при нормальных условиях. Например, чтобы синтетический катализатор произвел реакцию превращения атмосферного азота в аммиак, необходима температура в 400‘С и давление 4х107 Па. А в клетках азотфиксирующих клубеньковых бактерий эта реакция происходит при нормальных условиях.
- Кроме влияния стандартных условий (температуры, давления и т. д.), на работу биологических катализаторов сильнее влияют кислотность среды, наличие иных органических веществ и молекул. В целом это делает работу биологических катализаторов более сложной и управляемой большим количеством условий.
Активный центр фермента. Что же представляют собой ферменты по химической природе? Как уже было сказано, в основном, это вещества белковой природы. Значительное число ферментов - это так называемые
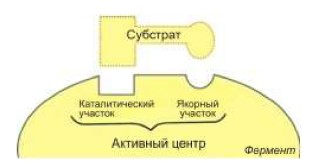
сложные белки, в состав которых, кроме аминокислот, входят другие элементы. Это могут быть ионы металлов (часто меди, цинка, кобальта, хрома, железа), неорганические кислоты или их остатки (например, пепсин содержит остатки фосфорной кислоты), витамины или их части, или какие-либо иные вещества (углеводы, липиды и т. д.). Неаминокислотную часть сложных белков называют простетической группой. Как правило, именно вещества простетическоЙ группы делают фермент активным. По этому принципу ученые-биохимики выделили понятие активный центр фермента. Это именно та его часть, которая непосредственно взаимодействует с «субстратом» - веществом-реагентом, вступающим в каталитическую ферментативную реакцию. Если в состав фермента входит простетическая группа, то это и есть активный центр фермента.
Что же определяет активный центр фермента? Два основных каталитических понятия - специфичность и скорость ферментативной реакции. Чтобы ярче проиллюстрировать, что активный центр фермента может взаимодействовать только (!) со строго определенным веществом-реагентом, говорят, что «они подходят друг к другу, как ключ к замку». Еще говорят о фермент-субстратном взаимодействии (рис. 18).
Если вы пробовали открывать дверь неподходящим ключом, то, наверное, понимаете, что это непросто, даже если ключи внешне похожи. Но если с замками все не так однозначно, можно, например, подобрать «универсальный ключ», т. е. отмычку, то на химическом уровне такое невозможно. Ферменты с большой долей вероятности «не откроют чужой замок».
Знание и понимание
- Что такое активный центр фермента?
- Как вы понимаете, что такое специфичность ферментов?
Применение
- Сравните биологические и небиологические катализаторы.
- Из чего могут состоять активный центр фермента и сам фермент? Анализ
Изобразите в виде схемы процесс ферментативной и (или) каталитической реакции соединения и разложения.
- Докажите на примерах, что ферменты высокоспецифичны.
Синтез
- Напишите эссе о работе разнообразных ферментов, приведите конкретные примеры.
- В чем состоит эволюционный смысл формирования ферментов? Какие преимущества для живого это имеет?
Оценка
- Оцените теоретическую возможность создания искусственного универсального фермента, катализирующего несколько жизненно важных реакций в клетке (организме). Возможно ли это? Почему такое вещество не воз и и к ло в ходе эволюции?
- Оцените значение скорости работы ферментов, проанализировав текст: «Известно, что реакция самоудвоения (синтеза) ДНК полимеризация мономеров в цепь происходит без участия фермента ДНК-полимеразы в присутствии катализаторов ионов цинка. Но скорость такой реакции 1 мономер (нуклеотид) в секунду. Скорость синтеза у бактерий 1000 мономеров в секунду, а у эукариот 100 мономеров в секунду».
Лабораторная работа № 2
Исследование влияния различных условий (температура. pH) на активность фермента
Цель работы: убедиться в работе пищеварительных ферментов па примере амилазы слюны.
Оборудование: вареный крахмал, йод, термостат(ы) или термос с горячей (55-60 С), умеренно-теплой (36 37,5 С), холодной (со льдом) водой, лимонная кислота, пищевая сода, йод, часы, водный термометр, набор пробирок и химических стаканов.
Ход работы
- В пробирки (6 штук) налейте по 2 3 мл чистой воды комнатной температуры
- Разделите пробирки по двум штативам (№ 1 и № 2). так как три из них будут использоваться для определения влияния pH на активность фермента, а три другие для выявления влияния температуры. Пробирки в каждом из штативов пронумеруйте.
- Начинать работу можно с любым из штативов. Для определения влияния pH в пробирку № 1 необходимо добавить немного лимонной кислоты (5 6 капель или маленькую щепоть), в пробирку № 2 добавить немного пищевой соды (5 6 капель или маленькую щепоть), пробирку № 3 оставить без изменений (контрольная).
- Во все три пробирки прилейте 2 мл раствора крахмала и примерно по 2 3 мл слюны (от одного человека).
- Все пробирки на 5 мин поместите в термостат при 37°С или в теплую воду, поддерживая температуру 36 38°С.
- Прилейте йод в пробирки, помешайте содержимое стеклянной палочкой.
- Понаблюдайте за изменениями, данные занесите в таблицу.
- Аналогичную работу проведите с пробирками из второго штатива, добавив в каждую из них крахмал и слюну в равных количествах и в одно время.
- Поместите пробирки (на 3-5 мин) в разные температурные условия: № 1 в холодную воду со льдом, № 2 - в горячую воду (55 60°С), № 3 в теплую воду 37 С (36 38°С). Примечание. В ходе выполнения работы для поддержания температуры может использоваться термостат. Если термостата нет в наличии, то пробирки помещаются в стаканы с водой заданной температуры, туда же опускается термометр и постоянство температуры поддерживается добавлением более теплой (горячей воды) или кубиков льда.
- Прилейте йод в пробирки, помешайте содержимое стеклянной палочкой.
- Понаблюдайте за изменениями, данные занесите в таблицу.
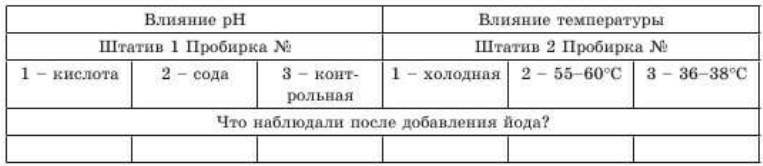
- Сделайте выводы по итогам наблюдений о влиянии pH и температуры на активность фермента амилазы.
§ 12. Эмульгирование жиров под действием желчи
Цель изучения этой темы, исследовать процесс эмульгирования жиров под действием желчи.
Где образуется желчь? Куда она поступает? Для чего нужна желчь?
Что нужно повторить для успешного изучения темы? § 12 - учебник биологии для 8 класса.
Желчь как производное самой крупной железы. Печень, как самостоятельный орган, впервые сформировалась у моллюсков. Как вы помните, это самая крупная железа у большинства млекопитающих, в том числе человека. Вес печени человека около 1,5 кг. Роль ее в организме многогранна. Секретом печени является желчь. За сутки у человека в среднем образуется 700-800 г желчи.
В состав желчи входят вода (97-98%), желчные кислоты, пигменты, придающие желчи характерный цвет, холестерин и другие вещества.
Учитывая, что печень играет важную роль в процессе утилизации состарившихся клеток крови, это не могло не сказаться на составе желчи.
Основным желчным пигментом является билирубин - вещество желтого цвета. Именно он окрашивает впоследствии не только желчь, но и каловые массы. Желчные пигменты синтезируются из железосодержащего гемоглобина, который высвобождается из состарившихся разрушенных эритроцитов.
Желчные кислоты синтезируются клетками печени (рис. 19). Кроме того, в желчи содержатся слизеподобные вещества, повышающие ее плотность и вязкость, жирные кислоты, неорганические вещества и т. д.
В клетках печени желчь образуется непрерывно. А вот ее поступление в двенадцатиперстную кишку происходит под действием нервных импульсов и активизируется во время пищеварения. Если человек не принимает пищу, желчь будет накапливаться в желчном пузыре. Накопившаяся в желчном пузыре желчь как бы «дозревает», т. е. становится менее водянистой, более плотной и концентрированной.
Роль желчи в пищеварении. Желчь выполняет разнообразные функции, например утилизацию веществ, образующихся при разложении эритроцитов. Это отличает желчь от других пищеварительных соков. Однако главная ее роль - это участие в пищеварении.
Желчь повышает активность ферментов сока поджелудочной железы. Без желчи кислая пищевая кашица, поступившая из желудка в двенадцатиперстную кишку, не стала бы сразу щелочной. То есть желчь помогает

процессу подщелачивания, чтобы облегчить работу ферментов поджелудочных амилазы и трипсина.
Главный фермент поджелудочной железы - липаза - вообще неактивна в отсутствии желчи. Это происходит не только из-за pH-среды. Желчь эмульгирует жиры. Желчные кислоты разбивают нейтральные жиры на огромное количество мельчайших капелек. Этот процесс и называется эмульгацией. Таким образом увеличивается площадь поверхности соприкосновения жира с молекулами фермента - липазы, и процесс расщепления жиров облегчается и ускоряется.
Желчь повышает активность как самой липазы, так и всей поджелудочной железы. Она усиливает сокоотделение, повышает тонус поджелудочной железы и стимулирует перистальтику кишечника, облегчает процесс пристеночного пищеварения на поверхности кишечных ворсинок.
Но на этом роль желчи в пищеварении не заканчивается. Она необходима для всасывания жирных кислот и, следовательно, жирорастворимых витаминов A, D, Е и К. Кроме того, желчь предупреждает гнилостные процессы в кишечнике. Она умеренно подавляет развитие вредной кишечной микрофлоры и безвредна для полезных симбиотических кишечных бактерий.
Знание и понимание
- Сколько желчи вырабатывается в сутки?
- От чего зависит процесс выделения желчи в кишечник?
Применение
- Из чего состоит желчь?
- Охарактеризуйте состав и значение желчи для организма.
Анализ
- Изобразите в виде схемы состав желчи и ее функции.
- Выскажите свое мнение о причинах активизации или торможения процесса выделения желчи в кишечник.
Синтез
- Систематизируйте по критериям все функции желчи. Все ли они связаны с пищеварением?
- Напишите эссе о роли желчного пузыря, о том, какие изменения произойдут в организме после его удаления.
Оценка
- Считаете ли вы, что рекомендации отказаться от жирной животной пищи для людей с ослабленной болезнями печенью оправданы? Ответ аргументируйте.
- Оцените значение следующих сведений, полученных в ходе исследований. Выявлено, что желчегонным эффектом обладают молоко, мясо, хлеб. У жиров это действие выражено в большей степени, чем у белков и углеводов. Обнаружено, что продолжительность желчевыделения на мясо равняется в среднем 7 ч, на хлеб 10 ч, на молоко примерно 9 ч. Желчь выделяется в большем количестве на мясо и молоко, в меныием на хлеб. Максимум секреции на мясо наблюдается на втором часу, на хлеб и молоко на третьем часу после приема пищи. Было также установлено, что наибольшее количество желчи выделяется при смешанном питании.
Лабораторная работа № 3
Исследование процесса эмульгирования
Цель работы: экспериментально ознакомиться с процессом эмульгирования жиров.
Оборудование: растительное масло, желчь, 1%-ный раствор куриного белка, 1%-ный раствор мыла, 1%-ный раствор щелочи (например, карбоната натрия Na2CO3), дистиллированная вода, штатив с пробирками, дозатор.
Необходимая теоретическая информация. Эмульгирование это процесс дробления крупной капли жира на мелкие. Известно, что жиры с водой образуют нестойкую эмульсию, которая при стоянии быстро расслаивается из-за того, что капельки масла собираются вместе на поверхности. Чтобы этого избежать, к эмульсии добавляют вещества (эмульгаторы), которые снижают поверхностное натяжение и препятствуют слиянию раздробленных, каплеобразных частиц жира. К таким веществам относятся белки, мыло, растворы щелочей и др. В организме основными эмульгаторами жира являются желчные кислоты, которые обеспечивают образование тонкой водно-жировой эмульсии.
Ход работы
- В штативе установите пять пробирок и пронумеруйте их.
- В каждую пробирку поместите по 2 капли растительного масла и по 1 мл дистиллированной воды.
- Затем добавьте в 1-ю пробирку 5 капель желчи, во 2-ю 5 капель раствора щелочи, в 3-ю 5 капель раствора мыла, в 4-ю 5 капель раствора белка, в 5-ю - 5 капель дистиллированной поды.
- Содержимое пробирок встряхивайте в течение примерно 1 мин с одинаковой частотой и интенсивностью.
- Наблюдайте за устойчивостью эмульсий на протяжении 1-10 мин.
- Эмульсия считается расслоившейся, если масло отделилось и образовало пленку па поверхности поды.
- Заполните таблицу.
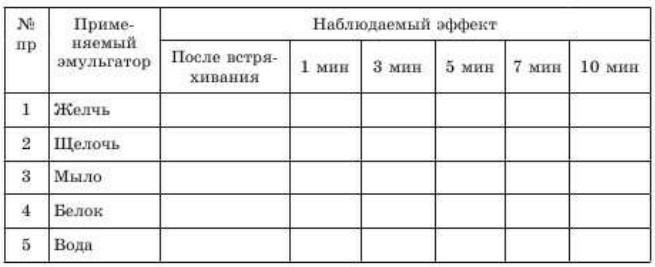
- 8. Укажите, с каким из эмульгаторов образовалась наиболее устойчивая эмульсия.
- 9. Сделайте вывод об эффективности эмульгирующих свойств применяемых реагентов и роли желчи в пищеварении.
