Химия для 11 класса — Оспанова М.К.

| Название: | Химия для 11 класса |
| Автор: | Оспанова М.К., Аухадиева К.С., Белоусова Т.Г. |
| Жанр: | Школьный учебник по химии |
| Издательство: | Мектеп |
| Год: | 2019 |
| ISBN: | |
| Язык книги: | Русский |
| Скачать: |
Страница - 4
§8. ХИМИЧЕСКИЕ СВОЙСТВА, ПРИМЕНЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
Сегодня на уроке:
- изучим свойства и применение альдегидов и кетонов.
Ключевые понятия
- альдегиды
- кетоны
- физические свойства
- химические свойства
- применение
Физические свойства. Альдегиды и кетоны — полярные вещества с избыточной электронной плотностью на атоме кислороде. Низшие члены ряда альдегидов и кетонов растворимы в воде. Их температуры кипения ниже, чем у соответствующий спиртов. Метаналь (формальдегид) — бесцветный ядовитый газ с резким запахом. Водный 35—40% раствор формальдегида называют формалином.
Остальные члены гомологического ряда альдегидов — жидкости, а высшие альдегиды — твердые вещества.
Ацетон — легколетуча я жидкость.
Химические свойства.
1. Реакции восстановления. Альдегиды и кетоны способны присоединять водород по двойной связи; альдегиды образуют при этом
первичные спирты, кетоны — вторичные:
Если, например, пары метаналя вместе с водородом пропускать над
нагретым никелевым катализатором, то происходит присоединение водорода. Формальдегид восстанавливается до метилового спирта.
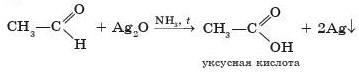
Подобные уравнения реакций можно составить и для других альдегидов.
- Реакции окисления.
Под влиянием карбонильного атома кислорода альдегиды окисляются по связи С—Н в альдегидной группе. Если в чистую пробирку налить аммиачный раствор оксида серебра Ag2O, прибавить к нему раствор альдегида и смесь осторожно нагреть, то на стенках про бирки появится блестящий налет серебра. В этой окислительно-восстановительной реакции альдегид превращается в кислоту, а серебро выделяется в свободном виде: